zurück zu Kapitel 1

Ein in einem Axon fortgeleitetes AP dient der Informationsweiterleitung an andere Neurone und Muskelzellen. Die Energiequelle für ein AP und ganz besonders auch für die Fortleitung des AP steckt bereits im EM (aufgeladener Kondensator).
1 Enstehungsort eines AP
Ein AP kann zum Beispiel entstehen:
) am Axonhügel von Nervenzellen durch räumliche und zeitliche Summation von EPSP und IPSP, die sich von der postsynaptischen Membran elektrotonisch zum Axonhgel ausbreiten.
Die Bezeichnung “ Ausbreitung” wird übrigens für einen passiven, elektrotonischen Vorgang, “ Fortleitung” für einen aktiven Fortleitungsmechanismus und “ Überleitung” für die Übertragung an Synapsen verwendet.
) am ersten Schnürring, generiert durch das Receptorpotential (Frage 26).
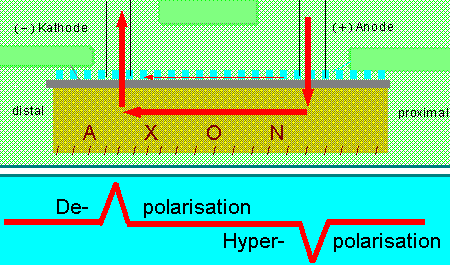
) durch elektrische Depolarisation über extracelluläre Elektroden (Praktikum, Frage 3 und 4).
Unter Depolarisation versteht man eine Abweichung des EM in positive Richtung, unter Repolarisation eine Rückführung zum EM, und Hyperpolarisation ist eine Abweichung des EM in negative Richtung.
nach oben
2 Auslösung eines AP’s – Schwelle
Wird eine Membran z.B. am Axonhgel durch räumliche und zeitliche Summation von EPSP und IPSP zur Schwelle, “firing level“, depolarisiert, so kann dort ein AP ausgelöst werden. Wenn die Schwelle über das Präpotential erreicht wird, kommt es schlagartig zu einer Änderung von g Na; es kommt zu einem
|
selbsttätigen,
|
|
|
| |
fortschreitenden
|
|
| |
|
Ladungsabbau
|
der auch Erregung genannt wird.
Da die Auslösungsursache und Häufigkeit (abgesehen von einer Auslösung in der relativen Refraktärphase) keinen wesentlichen Einfluss auf die Amplitude des AP hat, wird die Konstanz des AP auch als “Alles-oder-Nichts-Gesetz” der Erregung bezeichnet.
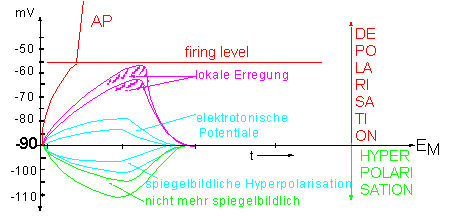
Bis zu einem gewissen Grad (einige mV) kann man eine Membran depolarisieren und ihr Verhalten bleibt dabei passiv; das heißt, wenn man die Reizelektroden umpolt (oder durch IPSP), so ergibt sich eine spiegelbildlich gleiche Hyperpolarisation. Es handelt sich um eine elektrotonische Depolarisation, wobei die Depolarisation dem Reiz proportional ist.
Abbildung 4: Lokale Erregung

Ab einer bestimmten, noch geringen Depolarisation kommt es zur lokalen Antwort, bei der, der Na+-Einstrom kurzfristig den K+-Ausstrom überwiegt;
es ergibt sich keine symmetrische Hyperpolarisation bei umgepoltem Reizstrom. Es handelt sich hier um eine lokale, ortsgebundene “Erregung”, die nicht fortgeleitet wird (Erregung ist nicht ganz korrekt, aber es sind bereits geringe aktive Prozesse beteiligt). Nur elektrotonische, passive Ausbreitung ist möglich.
Ab der Schwelle kommt es zu der selbsttätigen, fortschreitenden Entladung, dem AP.
Nur das AP wird aktiv fortgeleitet!
Ein elektrotonisches Potential und eine lokale Antwort können sich lediglich passiv ausbreiten, wobei Verluste auftreten – die Amplitude verringert sich.
Bei der aktiven Fortleitung eines AP hingegen bleibt sie praktisch gleich.
nach oben
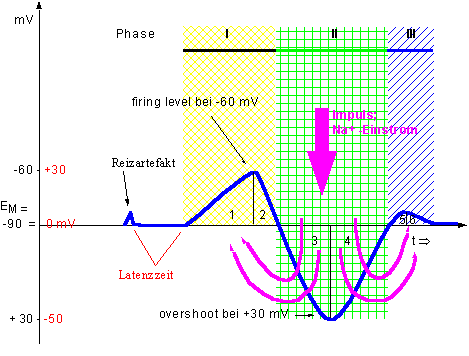
3 Zeitlicher Verlauf eines AP
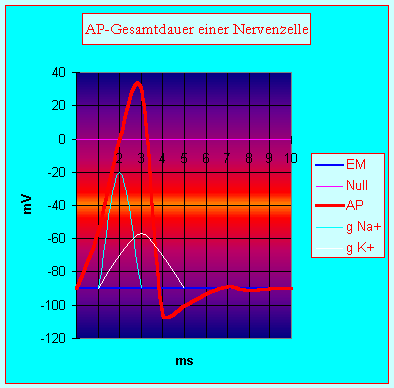
Diagramm 1: AP-Verlauf

Das AP setzt sich nach der Depolarisation zur Schwelle (-50 mV bis -60 mV) mit einer schnellen Aufstrichphase (ca. 0,2 bis 0,5 ms) fort, wobei die Membran die Polarisation verliert; daher auch Depolarisationsphase des AP.
Das Membranpotential wird dann sogar kurz positiv – und zwar in der Überschussphase (overshoot) und kehrt dann in der Repolarisationsphase zum EM zurck.
Depolarisiert wird die Membran durch einen schnellen Na+-Einstrom und repolarisiert wird sie durch einen langsameren K+-Ausstrom.
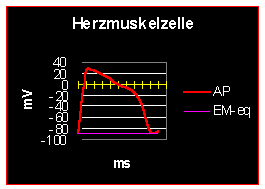
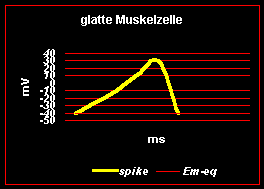
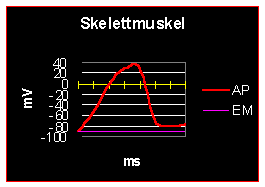
An der Schwelle ändert sich g Na+ und Na+ strömt wegen des elektrischen und chemischen Konzentrationsgradienten in die Zelle ein. Dadurch wird das EM positiver; es wird abgebaut; der Membrankondensator entlädt sich völlig. Wenn das EM positiver wird, bewirkt dies, dass die g K+ erhöht wird und K+ strömt (da jetzt der elektrische Gradient gering, der chemische Konzentrationsgradient aber sehr groß ist) aus der Zelle aus. Kehrt g K+ nicht schnell genug zum Ausgangswert zurck, so nähert sich das EM dem EK an und es kommt zu einem kurzen hyperpolarisierenden Nachpotential. Für längere hyperpolarisierende Nachpotentiale wird eine elektrogene Na-Pumpe verantwortlich gemacht. Beim Skelettmuskel kommt es z.B. in der letzten Phase der Repolarisation zu einer Verlangsamung, die als positives Nachpotential bezeichnet wird. Im folgenden ein paar Skizzen zu verschiedenen AP, die lediglich zum Vergleich dienen; nähere Angaben finden sie unter den jeweiligen Fragen:


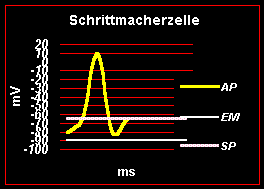
Beim Schrittmacherpotential ist das LDP (Langsames Diastolisches Potential) und das MDP (Maximales Diastolisches Potential) besonders zu beachten. Beim LPD weist die Steigung auf die Frequenz hin, mit der die AP ausgelöst werden.


nach oben
4 Refraktärphasen
Unmittelbar nach einer Depolarisationsphase eines AP, also wenn das EM noch nicht wieder erreicht ist, sind die Na-Kanäle nicht aktivierbar, wodurch es zu einer absoluten Refraktärphase kommt. Bei einer AP-Dauer von einer ms hat sich das Na+-System nach ca. 1-2 ms bereits etwas erholt, und es ist ein erneutes AP, allerdings mit geringerer Amplitude – relative Refraktärphase – auslösbar.
Nach ca. 4 ms ist das Na+- System wieder normal aktivierbar, und man kann ein normales AP auslösen. Die ungefähren Zeiten gelten für Nervenfasern; beim Herzmuskel liegen andere Verhältnisse vor. Wegen der langen APs findet man dort auch lange Refraktärphasen, welche dafür verantwortlich sind, dass das Herz nicht tetanisierbar ist.
Die theoretisch höchste Frequenz für des Myokards ist ca. 400/min;
für den AV-Knoten aber “nur” 230/min.
Die absolute Refraktärphase dauert bis zum Erreichen des EM an. Am Ende der Repolarisationsphase, wenn das EM wieder erreicht wird, folgt die relative Refraktärphase. Sie ist abhängig von etwaigen Nachpotentialen.
Die absolute Refraktärphase wirkt limitierend auf die Frequenz.
Na-Kanäle sind i.a. nur mit einer bestimmten Geschwindigkeit vom EM bzw. von einer Hyperpolarisation aus aktivierbar. Wesentlicher als die Geschwindigkeit ist aber das Ausgangspotential, von dem aus eine Erregung ausgelöst wird. Bei einer Erregung, die von -60 mV ihren Ausgang nimmt ist der Na+-Einstrom fast um die Hälfte kleiner, als bei einem Ausgangspotential von -100 mV.
Eine langsame Depolarisation zur Schwelle kann aber auch zu einer Inaktivation der Na-Kanäle und somit zur Unerregbarkeit der Membran führen.
nach oben
5 Elektrotonisches Potential (Elektrotonus) an langgestreckten Zellen
Folgendes ist nur im Bereich eines elektrotonischen Potentials gültig. Die Depolarisation muss also so gering sein, dass es zu keinem AP kommt: Die Membran verhält sich dabei passiv.
Eine solche elektrotonische Depolarisation findet man z.B. beim EPSP an der postsynaptischen Membran, wenn durch einen Transmitter die Leitfähigkeit für Na+ kurz geringfügig erhöht wird (g Na+ ). Nicht jedoch an der “Motorischen Endplatte“, denn das Endplattenpotential ist immer überschwellig -“Alles-oder-Nichts-Gesetz“.
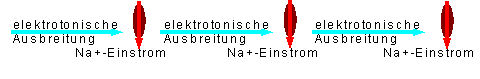
Ein elektrotonisches Potential kann man auch durch Applikation von positiven Ladungen in eine Nervenzelle erreichen. Bringt man in die Zelle positive Ladungen ein, so verringert sich die negative Ladung und das EM wird positiver; d.h. der Membrankondensator wird entladen, was nur über einen Widerstand, der im Vergleich die zwei Kondensatorplatten, bzw. Pole des Kondensators verbindet, möglich ist. Man denke an das Praktikumsbeispiel in Physik – “Entladung eines Kondensators”. Grob schematisch kann man sich die elektrotonische Ausbreitung wie unten skizziert vorstellen:
Skizze 1: Elektrotonische Ausbreitung

nach oben
5.1.Vergleiche zwischen Memraneigenschaften und Verhältnissen am technischen Kondensator
Wenn wir einen Kondensator, aus stilistischen Gründen möchte ich ihn mit Elko bezeichnen, an eine – der Einfachheit wegen – Gleichstromquelle schließen, so wird sich der Kondensator aufladen. Nehmen wir an, dass, wenn unser Elko voll aufgeladen ist, zwischen seinen Polen eine Spannung von 95 mV vorliegt. Nun entfernen wir den Kondensator aus dem Stromkreis, so dass sich zwischen seinen Polen nur Luft befindet. Diese hat bekanntlich einen extrem hohen Widerstand, weshalb sich der Kondensator praktisch nicht entladen kann (zumindest nicht in einer relevanten Zeit).
Für die Membran – Kondensatorladung, die wir bei gegebenem EM finden, sind statt der Batterie, hs. die verschiedenen, potentialabhängigen Leitfähigkeiten, die verschiedenen Gleichgewichtspotentiale der Ionen (EIon) und die direkte Wirkung der Na-K-Pumpe verantwortlich.
Bei unserem Elko, den wir geladen aus dem Stromkreis genommen haben, ist zwischen den Polen nun ein derart hoher Widerstand (Luft), dass er seine Ladung beibehält.
An der Membran finden wir im Ruhezustand eine derart geringe Ionenleitfähigkeit g (Ion), die diesem hohen Widerstand an Elko entspricht (g = 1/R).
Daraus folgt, dass das EM erhalten bleibt. Wird nun an der postsynaptischen Membran durch einen Transmitter g Na+ kurze Zeit geringfügig erhöht, so resultiert ein EPSC, d.h. Na+ strömen ein (man kann statt dessen experimentell auch Kationen in die Zelle einbringen, also positiven Strom applizieren). Durch den EPSC wird das Membranpotential positiver, also depolarisiert.
An unserem Elko wäre diesem Vorgang das Verbinden der Pole mit einem großen, aber nicht mehr so extrem großen R wie Luft ihn aufweist, gleichzusetzen. Elko kann sich dann, da R groß ist, nur langsam entladen und wenn wir diesen Vorgang unterbrechen (an der Membran kommt der Unterbrechung die Wiederherstellung der ursprnglichen, extrem geringen g Na+ gleich), bleibt der Kondensator nun praktisch auf diesem “neuen” Niveau. Schließt man Elko nun wieder an unsere Stromquelle, so wird er sich, nun von diesem Niveau aus, erneut aufladen und man kann dann wieder die ursprngliche Spannung zwischen seinen Polen vorfinden. An der Membran wird dies durch die erhöhte g K+ und durch die Na-K-Pumpe bewirkt.
Durch das sich in positive Richtung bewegende Membranpotential steigt die g K+ bei Na+-Zufuhr oder K+ Applikation. EIon wird dadurch wieder hergestellt und das EM wird erreicht. Falls experimentell der Kationenstrom weiterhin kontinuierlich in die Zelle geleitet wird, so kann das Ausgangspotential aber nicht wieder hergestellt werden, sondern es stellt sich ein Gleichgewicht zwischen eingebrachten und ausströmenden Kationen ein und das Membranpotential wird auf dem “neuen” Niveau gehalten.
Würde man Elko statt mit einem großen mit einem sehr kleinen R kurzschließen, so könnte er sich in sehr kurzer Zeit völlig entladen. An der Membran entspräche dies der schlagartigen Vergrößerung von g Na+, doch kommt dort bei einem AP ein weiterer Faktor hinzu, den man auch bei gröbster Vereinfachung nicht übergehen sollte, denn bei einem AP kann es ja zu einer Ladungsumkehr kommen, was bei einer Kondenstorentladung nicht ohne weiteres möglich ist (siehe Punkt 2.6).
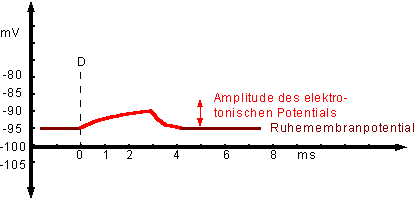
Der Potentialverlauf, dem der EPSC zugrundeliegt und der auch bei einer Kondenstorentladung zu beobachten ist, (im Diagramm “Potentialverlauf” oben rechts von D) wird elektrotonisches Potential oder Elektrotonus genannt.
Diagramm 2: Potentialverlauf

Dieses elektrotonische Potential, betrachten wir es nun einmal isoliert, nimmt im gleichen Ausmaß zu wie das Membranpotential abnimmt, d.h. es entspricht der De-Polarisierung.
Charakteristisch und von wesentlicher Bedeutung ist der exponentielle Verlauf des Potentials, dem der kapazitive Strom zugrunde liegt. Der Exponent, sagen die Physiker, ist dabei -t/t. Bei t (tau) handelt es sich um die sogenannte Membranzeitkonstante, wobei t = R.C
Die Membranzeitkonstante (t) ist das Produkt aus Membranwiderstand mal Membrankapazität.
Bei großem t, z.B. wegen eines großen R, kann sich ein Kondensator nur langsam auf- bzw. entladen und man findet ein flach verlaufendes elektrotonisches Potential.
Für die Spannung Uc, die zur Zeit t an einem Kondensator anliegt, gilt
Gleichung 7: Spannung zur Zeit t

dabei stellt I0 R e -1t/RC den zeitlichen Verlauf des an R auftretenden Spannungsabfalls dar.
Für den Entladevorgang kann man daher an Elko zur Zeit t die Spannung Uc finden, mit:

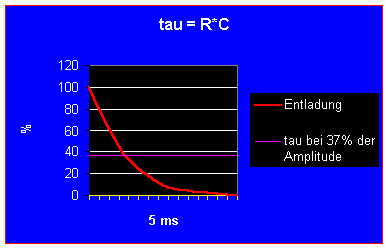
Um t festzustellen wird sie bei 37% der Amplitude der Entladekurve abgelesen. Dies ist möglich, da für t ist t der Exponent zu -1 wird. Es ergibt sich daraus e-1 = 1/e = ,718 = 0.36791758646063 0,37; d.h. Uc = U0 * 0,37; deshalb kann t bei 37 % der Amplitude abgelesen werden; (e = Euler’sche Zahl, die Basis von ln).
Diagramm 3: Membranzeitkonstante

Das Diagramm zeigt den Verlauf eines elektrotonischen Potentials an der Zellmembran bei gleichbleibender, geringer, kontinuierlicher Kationen – Applikation (U könnte z.B. 5 mV sein, 100% wären z.B. -95 mV und 0% -90 mV), bzw. die Entladekurve eines Kondensators, mit eingezeichneter (Membran-) Zeitkonstante.
Durch die Störung des Ionengleichgewichts (Zufuhr pos. Ldg.)beginnt allmählich K+ aus der Zelle auszuströmen, und bald fließen gleich viele pos. Ladungen aus der Zelle wie zugeführt werden. Das bedeutet, der Membrankondensator entlädt sich ständig langsamer, bis gleich viele Ionen bidirektional fließen, dann bleibt er auf diesem Niveau und wird nicht weiter entladen; anders bei einem AP; hier muss der depolarisierende Na+-Einstrom den K+-Ausstrom und die Na-K-Pumpen-Aktivität überwiegen, so dass die Schwelle erreicht werden kann und es infolge dessen zu einer selbsttätig fortschreitenden Entladung kommen kann.
Je nach Zelle kann t Werte zwischen 5 und 50 ms annehmen;
im Beispiel oben ist t (tau) 18 ms;
d. h. nach 18 ms ist die Amplitude auf 37 % verringert.
Wird nun an einer definierten Stelle an der postsynaptischen Membran die g Na+ erhöht, so wird sich der Membrankondensator zuerst in unmittelbarer Umgebung entladen. Dann aber breitet sich das elektrotonische Potential unter Verlust (siehe current sink – current – source – Modell) entlang der Membran aus, um in entfernteren Gebieten den Membrankondensator (nun natürlich weniger) zu entladen. Dabei ist ein Längswiderstand zu überwinden, wodurch das elektrotonische Potential flacher wird (abnimmt). Je größer dieser Längswiderstand (in der Membranlängskonstante enthalten) ist, um so langsamer wird sich der Membrankondensator entladen. Wegen des Verlustes muss sich natürlich auch die Amplitude des elektrotonischen Potentials mit zunehmender Entfernung verkleinern. Diese Verkleinerung mit dem Abstand s, wie könnte es anders sein, folgt wieder einer exponentiellen Funktion, wobei der Exponent -s/l ist. l wird dabei als Membranlängskonstante bezeichnet.
Noch einmal: Da sich ein elektrotonisches Potential unter Verlust ausbreitet (keine aktive Fortleitung!), fällt die Amplitude mit zunehmendem Abstand (s) vom Reizort bzw. Ausgangspunkt exponentiell ab; der Exponent ist -s/l. Nach einem l ist die Amplitude des elektrotonischen Potentials also um 63% abgefallen, nach zwei l schon um 86% usw.
Die Membranlängskonstante ist der Leitungsgeschwindigkeit proportional und dem inneren Membranwiderstand umgekehrt proportional. Elektrotonische Potentiale sind am Nerv also höchstens in cm – Entfernung vom Ursprung meßbar. Darüber hinaus werden sie auch noch durch die Na-K-Pumpe verkleinert.
nach oben
6 Current sink – current source Modell
Current sink – current source – Modell: Stromsenke und Stromquelle;
jeder Strom (auch die Donau) fließt von einer Strom – Quelle zu einer Strom – Senke.
“The current sink” zieht positive Ladungen ab;
“the current source” stellt sie zwangsweise zur Verfügung.
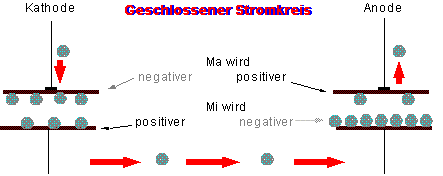
Durch den Na+-Einstrom wird das EM kurz umgepolt, wofür man im Schema eine negative Ladung an der Membranaußenseite zeichnen kann. Durch die außen fehlenden pos. Ladungen an der Stelle des AP und durch den geänderten Potentialgradienten entlang der Membranaußenseite, werden aus der Umgebung, an der Membranaußenseite, pos. Ladungen abgezogen. In der Skizze müssen sie daher an dieser Stelle (current sink) verdünnt eingezeichnet werden. An der Membraninnenseite finden sich an der Stelle des AP die eingeströmten pos. Ladungen. Da sich gleiche Ladungen abstoßen und ungleiche anziehen, wird wieder ein current source und ein current sink, nun aber an der Membraninnenseite, entstehen.
Die positiven Ladungen fließen bzw. übertragen den Impuls auf andere pos. Ladungen in Richtung des current sinks, also weg von der Stelle des Einstroms. Dabei wird die Membran etwas depolarisiert (man betrachte nun wieder den Potentialgradienten über die Membran; Außenseite – Innenseite) und dadurch werden pos. Ladungen (K+) durch die Membran nach außen sickern (Verlust), da nach geringer Depolarisation ja K+ ausströmen, wie beim “Elektrotonus” und bei der Frage “Das Ruhemembranpotential” erörtert wurde. Die Membran wird neben der Stelle des Na+-Einstroms elektrotonisch depolarisiert und zwar durch den Na+-Abzug außen und der Na+-Ansammlung, bzw. Verteilung, innen. Wird dabei die Schwelle erreicht, und dies ist normal bei einem fortgeleiteten AP der Fall, so kommt es an den Na-Kanälen der Umgebung, an der die Schwelle erreicht wurde ebenfalls zum Einstrom, das AP wird also fortgeleitet. Wegen der Refraktärphase ist dies nur mehr in eine Richtung möglich, denn wo vorher der Impuls war, ist ja nun die Membran kurz unerregbar (Inaktivation der Na-Kanäle; noch erhöhte g K+). Die Wiederherstellung der Ionengradienten durch die Na-K-Pumpe ist für das einzelne AP unwesentlich.
nach oben
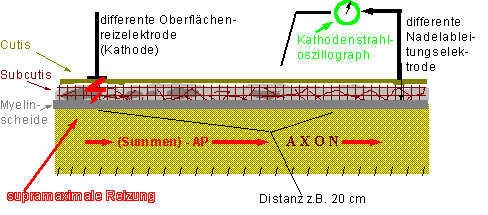
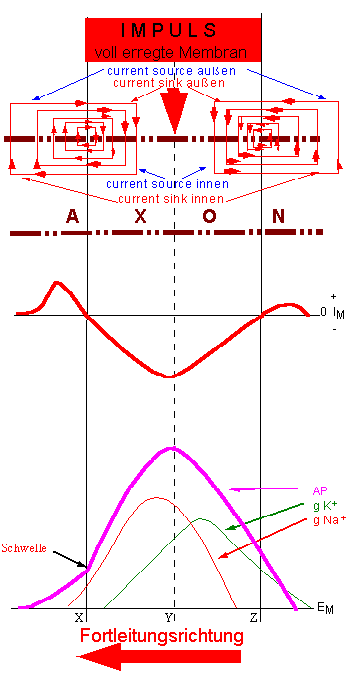
7 Verhältnisse während der AP-Fortleitung
Abbildung 5: AP-Fortleitung

Zwischen X und Z ist die Membran voll erregt; bei einer AP-Dauer von 1 ms müßte ein AP (auch ein Summenpotential) daher 10 cm lang sein, wenn die NLG 100 m/s beträgt; siehe Frage “NLG”. Zwischen X und Z überwiegt der Einstrom positiver Ladungen, die dann in beide Richtungen im Faserinneren abfließen, bzw. abgezogen werden.
Der a+-Strom wird an der Membranaußenseite abgezogen und verteilt sich an der Membraninnenseite, wodurch die Membran elektrotonisch depolarisiert wird. Dabei wird das EM positiver, wodurch die g K+ erhöht wird. Dadurch kommt es zu dem Verlust der elektrotonischen Ausbreitung (K+-Ausstrom).
Die Stromquelle für die Na+-Verteilung liegt im erregten Bezirk der Membraninnenseite. Die Anfangsphase des AP ist also hs. elektrotonisch bestimmt und die Fortleitungsgeschwindigkeit ist daher v. a. von t und l abhängig. Der Ausstrom hinter dem AP kann die Membran nicht zur Schwelle depolarisieren, da g K+ noch erhöht ist und weil die Na-Kanäle noch inaktivierbar sind (absolute Refraktärphase). Der Membranstrom (IM) ist die Grundlage für extracelluläre Ableitungen.
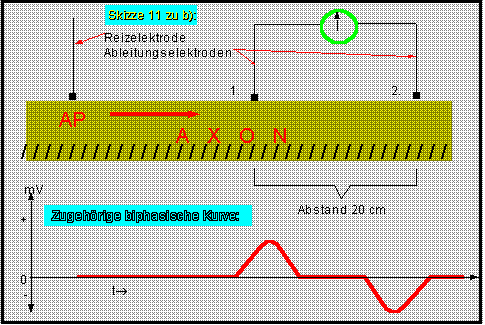
Die Elektroden messen die Stromdichte in der ECF, es werden daher dem IM proportionale triphasische spikes gemessen.
Beim fortgeleiteten AP fließt an der Spitze des AP (also wenn die Amplitude erreicht ist) noch ein starker Na+-Strom einwärts.
Dieser Strom ist für die elektrotonische Ausbreitung erforderlich.
) An markhaltigen Nerven breitet sich das AP saltatorisch – vom Ranvier’schen Schnürring zu Schnürring aus, wobei es an jedem Schnürring zu einen Na+-Einstrom kommt.
Daher bleibt die Amplitude während der Fortleitung über die gesamte Länge eines Axons praktisch gleich groß. An den Ranvier’schen Schnürringen liegen die Na-Kanäle besonders dicht. Der Membranwiderstand ist durch die Myelinscheide erhöht, wodurch die elektrotonische Ausbreitung besonders weit ausgreifen kann.
Da bei der elektrotonischen Ausbreitung nicht alle Ladungen jedesmal von der Quelle zur Senke fließen müssen, sondern ein Impuls weitergegeben werden kann (Ladungen im elektrischen Feld), findet die Ausbreitung über die Internodien ohne Zeitverlust statt. Die saltatorische Fortleitung eines AP läuft daher besonders schnell ab.
(Vergleich: wenn Sie eine entfernte Lampe einschalten, so wird diese sofort leuchten, obwohl die Elektronen z.B. erst einige cm weit durch das Potential getrieben wurden).
nach oben
8 Impulsserien durch langandauernde Depolarisation
In Nervenfasern werden nur AP aktiv fortgeleitet.
D.h., man spricht nur dann von einem AP, wenn der Na+-Einstrom ausreichend ist, um an den nächsten Na-Kanälen (z.B. am nächsten Schnürring) das EM bis zur Schwelle zu depolarisieren – sonst handelt es sich um eine lokale Erregung und nicht um ein AP. Die Frequenz enthält dabei die Information. An Sensoren und Nervenzellensomata (postsynaptische Membran – Axonhgel) summieren sich die synaptischen elektrotonischen Potentiale auf und werden zur Informationsweiterleitung in AP-Frequenzen codiert.
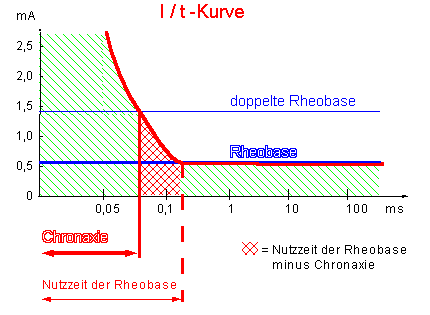
Wird z.B. mit 1 mA dauerdepolarisiert, so kommt es zu einer AP-Frequenz von ca. 4 Hz;
verwendet man 2 mA zur Dauerdepolarisation, so kommt es zu einer rhythmischen AP-Frequenz von ca. 7 Hz.
Die Anstiegssteilheit des Präpotentials(abhängig von R.C, also von t) ist ausschlaggebend für die Frequenz.
Durch Adaption kommt es zu einer langsamen Abnahme der Frequenz bei gleichbleibendem Reizstrom. Auf Dauerdepolarisation folgt also eine AP-Serie, wobei u.a. die Steilheit des Präpotentials die Frequenz bestimmt. Die Steilheit ist z.B. abhängig von der räumlichen und zeitl. Summation, von der Größe der EPSP und IPSP und deren Verhältnis.
Auch das verzögerte Anschalten des repolarisierenden K+-Ausstroms kann nach der Repolarisation wieder eine Depolarisation zur Schwelle bewirken und so eine rhythmische AP-Serie ermöglichen.
Ein verzögertes Abschalten hingegen bewirkt eine Hyperpolarisation und damit eine Erniedrigung der Frequenz. Bei der Umcodierung sind aber auch andere K+-Kanaltypen beteiligt. Ein K+-Ausstrom, der durch Depolarisation schnell inaktiviert wird, – wie der Na+-Einstrom – und erst wieder nach kurzer Hyperpolarisation aktiviert wird, verhindert so eine schnelle Depolarisation und wirkt damit auch vermindernd auf die Frequenz ein. Siehe auch “Schrittmacherzellen des Sinusknotens”.
Normal bewirkt eine Erhöhung der g K+ einen K+-Ausstrom, wodurch das Membranpotential negativer wird.
Bei der elektrotonischen Ausbreitung verteilen sich die eingeströmten pos. Ladungen an der Membraninnenseite, wodurch das Membranpotential positiver wird (also elektrotonisch depolarisiert wird) und daher können K-Ionen nach außen sickern (Verlust).
Es sei hier auch noch angemerkt, dass durch Lokalanästhetica oder Tetrodotoxin die Na-Kanäle blockiert werden können, wodurch die Fortleitung eines AP verhindert werden kann.
nach oben
9 Zwischenfragen:
- Zeichnen sie einen AP-Verlauf auf!
- Wie wird das firing level erreicht?
- Wo liegt in etwa die Zndschwelle?
- Warum kommt es zum Na+-Einstrom?
- Wie erfolgt die Aktivation der Na-Kanäle?
- Was wissen Sie über elektrische und chemische Konzentrationsgradienten?
- Erklären Sie die Leitfähigkeiten ( g Na+ und g K+)!
- Was folgt dem overshoot?
- Wie wird die Repolarisation eingeleitet?
- Warum kommt es zu einem K+-Ausstrom?
- Was ist ber die Dauer von APs zu sagen?
- Was ist die absolute, und was die relative Refraktärphase?
- Wie wird ein AP fortgeleitet?
nach oben
10 Weblinks:
Ein sehr schönes und meiner Meinung gutes pdf, dass Google mit https://www.google.at/url?sa=t&rct=j&q=&esrc=s&source=web&cd=2&cad=rja&uact=8&ved=0CCkQFjAB&url=https%3A%2F%2Fwww.neurobiologie.fu-berlin.de%2Fmenu%2Flectures-courses%2Fwinter-0708%2F23%2520118%2520Grundkurs%2FErregungsleitung_Synapsen0708_1Nov_compressed.pdf&ei=KPTIU4q0LobMOZ7lgLAM&usg=AFQjCNHfEQY4Uv2_RH15Bxh913qgUi0NLA&sig2=qLEodGsS_xBpwypD5hkCgQ&bvm=bv.71198958,d.ZWU findet. Also offensichtlich von https://www.neurobiologie.fu-berlin.de/ stammt, aber leider keine Angabe über Urheber, Autor und Lizenzrecht beinhaltet.
conduction membrane potential (pub Med Suche)
YouTube Video (Aktionspotential- Weiterleitung):
Die bearbeiteten Prüfungsfragen sind jetzt auch als Kindle Buch erhältlich.
Falls Interesse besteht, werde ich die Fragen neue überarbeiten und ergänzen. Daher freute ich mich besonders über Kritik, Anregungen, Ergänzungen und vor allem weitere Zwischenfragen, wie sie tatsächlich bei Prüfungen gestellt werden, bei den jeweiligen Fragen im Kommentarbereich.
zurück zu Kapitel 1